科技日報記者 張夢然
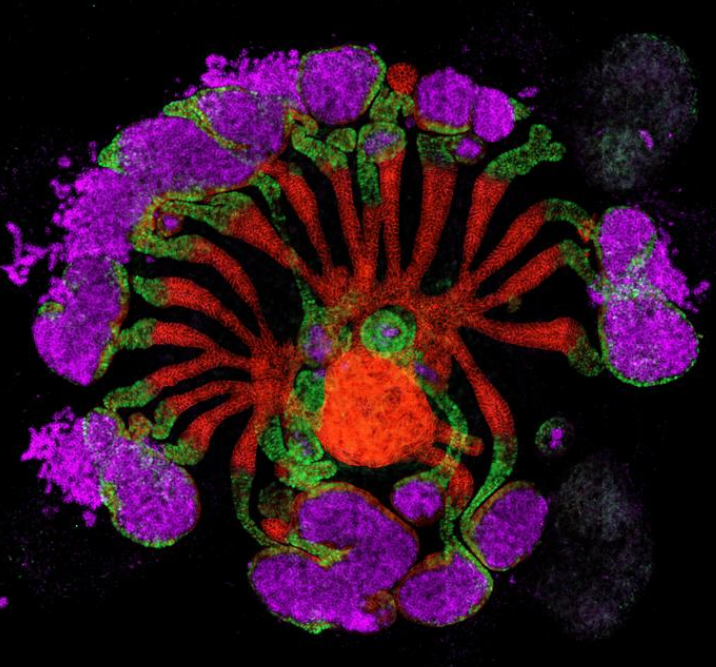
一組國際聯合研究團隊在構建合成腎臟方面取得重要突破:他們首次將腎臟關鍵結構整合,創造出被稱為“組合體”的新型腎臟組織。發表于最新一期《細胞·干細胞》雜志的這項成果,意味著人們成功培育出比以往更成熟、更復雜的腎臟類器官,為疾病研究和器官移植帶來新希望。
此次,包括美國南加州大學、俄克拉荷馬大學、南佛羅里達大學等多家美國研究機構聯合中國同濟大學組成的團隊,在實驗室中優化了小鼠和人類腎臟“組合體”的生長條件,隨后將其移植到活體小鼠體內。在生物體內天然環境的作用下,這些“組合體”進一步發育成熟,體積增大,并形成了結締組織和血管網絡。
移植后的“組合體”展現出多種類似真實腎臟的功能,包括血液過濾、吸收白蛋白等蛋白質、分泌腎源性激素,以及出現尿液生成的早期跡象。值得注意的是,以往的腎臟類器官通常只能發育到胚胎階段,而此次的“組合體”在基因活性和組織結構上已達到與新生小鼠腎臟相當的成熟水平。人類“組合體”也實現了超越胚胎階段的成熟,不過由于缺乏新生人類腎臟樣本,其確切成熟度尚難精確評估。
該研究還證明了“組合體”作為疾病模型的巨大潛力。團隊利用攜帶PKD2基因功能缺失突變的細胞培育出人類“組合體”,這種突變會導致常染色體顯性多囊腎病(一種以腎臟形成多個大囊腫并最終喪失功能為特征的遺傳性疾病)。此次這些患病“組合體”在小鼠體內發育出大型人源腎囊腫,并表現出炎癥和纖維化等復雜病理特征,而這些在以往的體外模型中都難以重現。
團隊表示,這不僅為研究多種復雜的腎臟疾病提供了一個強大的新工具,也為未來設計出可移植的功能性合成腎臟奠定了堅實基礎,更有望為無數等待腎移植的終末期腎病患者帶來新選擇。
總編輯圈點
這項研究的意義遠超實驗室成果本身,它標志著再生醫學向解決器官短缺危機邁出了實質性一步。通過構建功能更成熟、結構更完整的合成腎臟組織,科學家不僅為研究多囊腎等復雜疾病提供了前所未有的高保真模型,更重要的是驗證了一條通往功能性器官再生的可行路徑。一旦技術成熟,這類“組合體”有望成為個性化藥物測試平臺,可減少對動物實驗的依賴,并最終發展為可移植的生物“人工腎”,從根本上改變終末期腎病患者的治療格局,重塑現代醫學對器官衰竭的應對方式。




 網友評論
網友評論